31 mei 2025
De batterij werd ontdekt door Alessandro Volta in 1800. Dit was een belangrijk moment in de geschiedenis van elektriciteit en is niet meer weg te denken uit ons leven. Zo kan een smartphone niet werken zonder batterij.
Een batterij is een soort elektrochemische cel. In de kern bestaat een batterij uit drie hoofdonderdelen:
1. Twee elektroden – een positieve elektrode (de kathode) en een negatieve elektrode (de anode).
2. Elektrolyt – een stof die ionen geleidt, waardoor een elektrische stroom kan vloeien tussen de elektroden.
Hoe werkt een batterij?
Wanneer de batterij wordt gebruikt (ontladen), vinden er chemische reacties plaats aan de elektroden:
Bij de anode:
• De anode geeft elektronen af (oxidatie).
• Hierdoor komen ionen vrij in de elektrolyt.
Bij de kathode:
• De kathode neemt elektronen op (reductie).
• Tegelijkertijd worden ionen uit de elektrolyt gebruikt.
Elektrische stroom:
• De elektronen die van de anode komen, moeten een pad buiten de batterij volgen (via de draden naar bijvoorbeeld een lamp of telefoon).
• Dit pad heet de elektrische stroomkring.
Opladen en ontladen
• Ontladen: De batterij levert stroom aan een apparaat. De chemische energie wordt omgezet in elektrische energie.
• Opladen (bij oplaadbare batterijen): De chemische reactie wordt “teruggedraaid” door elektrische energie toe te voegen. De batterij kan dan opnieuw worden gebruikt.
Vandaag het de laatste dag van de meteorologische lente en doet de zomer al haar intrede met flink wat zon. Zoals gisteren met een productie van 33,7 kWh.
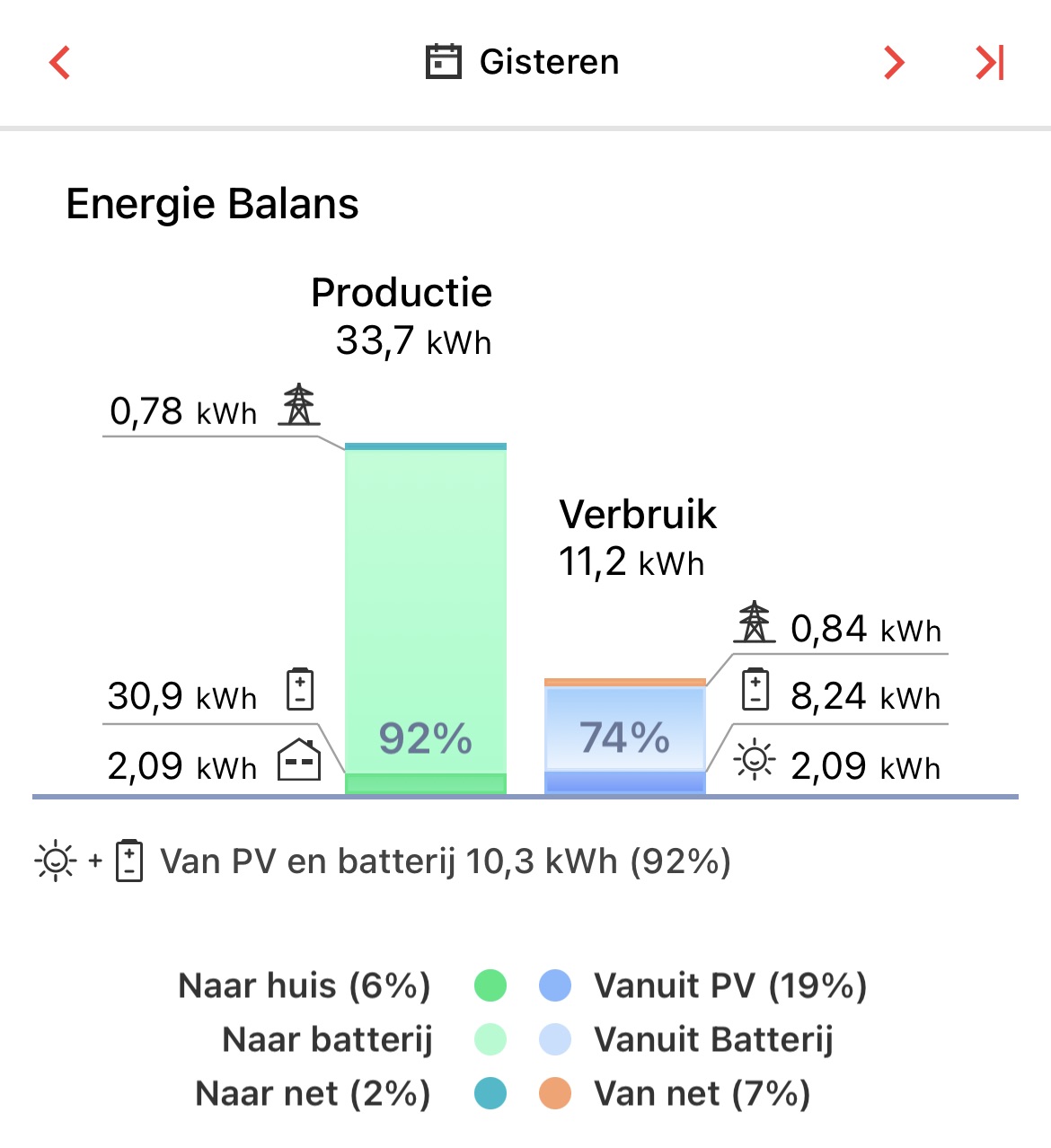
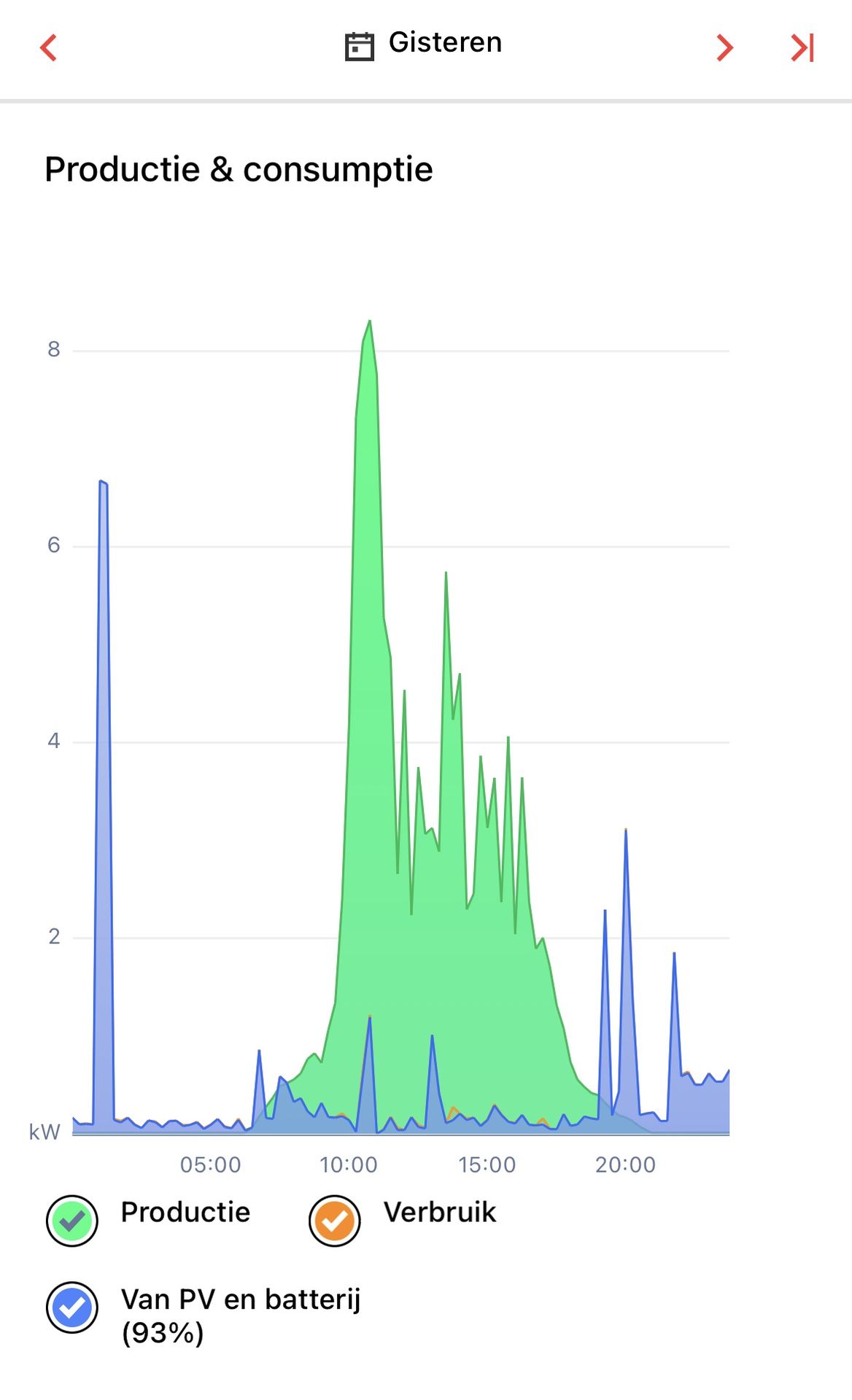
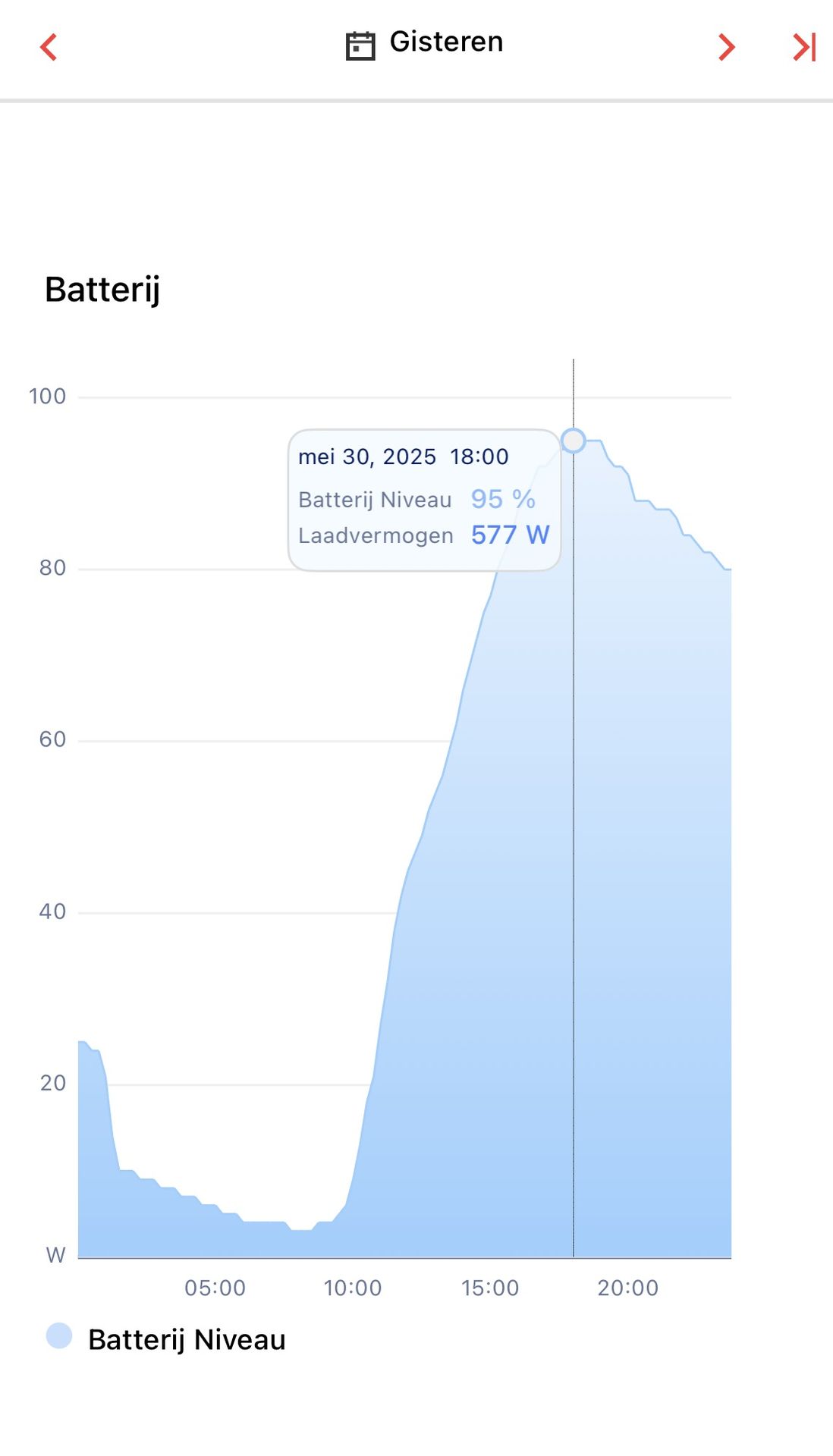
Gisteren de batterij tot 95% vol geladen. Morgen weten we wat vandaag gaat brengen.


